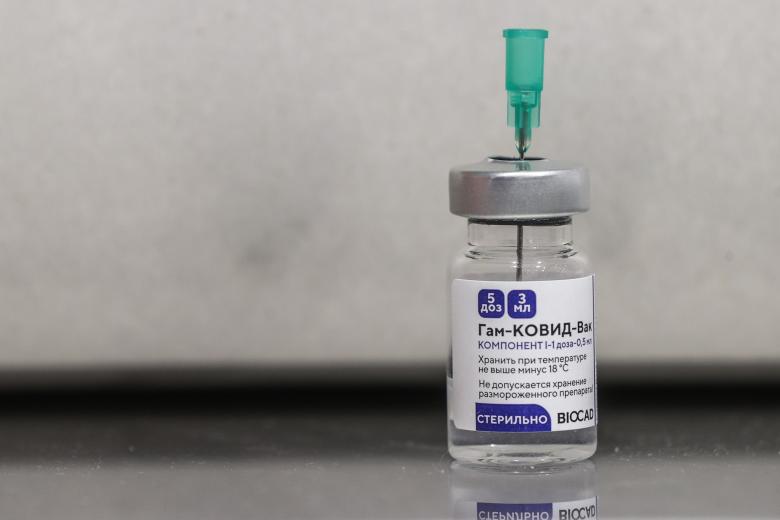
Регулятор ЕС завершил научное консультирование по российской вакцине от коронавирусной инфекции «Спутник V». Теперь разработчик может подать заявку на регистрацию препарата в Евросоюзе.
Лекарственным регулятором ЕС является Европейское агентство по лекарственным средствам (ЕМА). Представитель организации подчеркнул, что процесс научного консультирования облегчает компаниям подготовку программ разработки препаратов.
На данном этапе мы можем сказать, что Национальный исследовательский центр эпидемиологии и микробиологии имени Н. Ф. Гамалеи получил научную консультацию от ЕМА по разработке их вакцины для предотвращения COVID-19 «Спутник V» (известной также как Gam-COVID-Vac). В качестве следующего шага компания может подготовить заявку на получение регистрационного удостоверения (marketing authorisation), — приводит РИА Новости слова представителя ЕМА.
Он также отметил, что заявка от разработчика российской вакцины пока не поступала. Только после заявки можно будет обсуждать сроки получения одобрения от ЕМА для европейского лекарственного рынка. Если условное регистрационное удостоверение будет получено, а Еврокомиссия даст одобрение, то появится возможность для централизованных поставок «Спутника V» в Евросоюз. На данный момент в ЕС заключены контракты с шестью производителями вакцин от коронавируса.
Как ранее писал NEWS.ru, Всемирная организация здравоохранения (ВОЗ) допускает, что российский препарат «Спутник V» окажется в числе вакцин, которые распространяются по программе COVAX. Для этого он должен получить одобрение ВОЗ для использования в чрезвычайных ситуациях.
Программа COVAX сейчас имеет соглашения с производителями вакцин из Pfizer/BioNTech и AstraZeneca. Этим международным механизмом предусмотрено субсидирование закупок препаратов небогатыми государства за счёт оплаты вакцин странами с высоким уровнем доходов.